Anvisa autoriza: Brasil vai testar vacina de Oxford contra covid
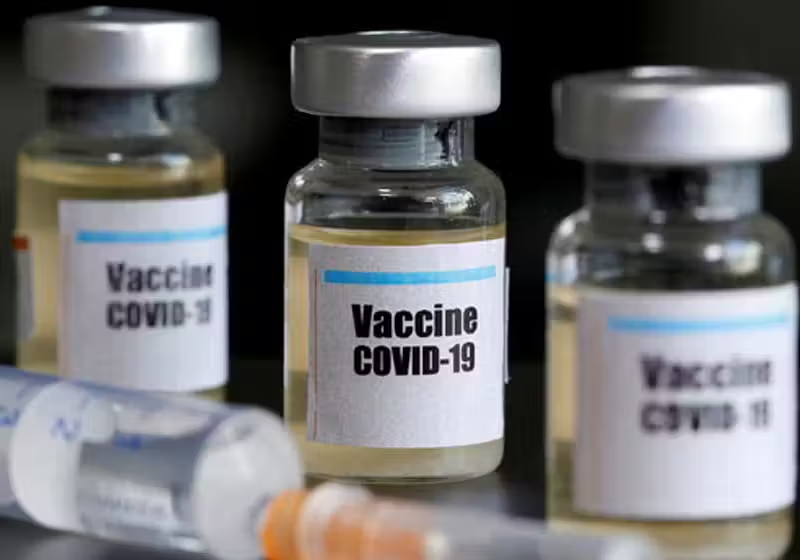
O Brasil vai participar dos testes mundiais da vacina de Oxford contra a covid-19. A autorização foi dada pela Anvisa – Agência Nacional de Vigilância Sanitária – e saiu em edição extra do Diário Oficial da União desta terça, 2.
O imunizante, que começou a ser testado esta semana em humanos na Inglaterra, será aplicado em 2 mil voluntários brasileiros que não entraram em contato com o novo coronavírus. No total, 10 mil pessoas no mundo inteiro vão participar dos testes.
No Brasil, segundo o Ministério da Saúde, os testes serão iniciados ainda neste mês.
As doses serão administradas em voluntários de São Paulo e do Rio de Janeiro, os dois estados que concentram o maior número de infectados.
No estado paulista, o CRIE – Centro de Referência para Imunobiológicos Especiais – da Unifesp – Universidade Federal de São Paulo – será o responsável por conduzir os estudos clínicos, que contam com o apoio financeiro da Fundação Lemann.
Segurança
Em nota oficial, a Anvisa falou sobre a segurança da vacina a ser testada:
“Os estudos iniciais não clínicos em animais e os estudos clínicos de fase 1 em humanos, para avaliar a segurança da vacina, foram realizados na Inglaterra e os resultados demonstraram que o seu perfil de segurança foi aceitável”, explicou a Anvisa em nota oficial.
O imunizante é considerado o mais avançado e um dos mais promissores, entre os mais de 70 que estão em desenvolvimento no mundo.
À frente da testagem na Escola de Medicina Tropical de Liverpool, está a imunologista brasileira Daniela Ferreira, de 37 anos, que o SóNotíciaBoa mostrou ontem.
Daniela explicou que a aposta nela é tão grande que, mesmo antes de aprovação, a vacina de Oxford já está sendo produzido em larga escala.
“Passamos da fase um para a fase três em apenas dois meses”, afirmou a brasileira.
A intenção é ter já o maior número possível de doses prontas para distribuição assim que o produto for aprovado e evitar um possível novo atraso na proteção da população mundial.
O processo de produção foi acelerado por que a vacina de Oxford já havia sido parcialmente testada em estudos feitos para a SARS (Síndrome Respiratória Aguda Grade) e a Mers (Síndrome Respiratória do Oriente Médio), também causadas por coronavírus.
Com informações do R7

 Alzheimer: brasileira ganha prêmio internacional por estudo revolucionário
Alzheimer: brasileira ganha prêmio internacional por estudo revolucionário Adolescente com autismo faz desabafo sobre sua condição e emociona a turma da escola; vídeo
Adolescente com autismo faz desabafo sobre sua condição e emociona a turma da escola; vídeo Artista brasileiro faz mini escultura linda do Papa Francisco; homenagens no dia do adeus
Artista brasileiro faz mini escultura linda do Papa Francisco; homenagens no dia do adeus Cãozinho faz ensaio fofo para foto do RG Animal e encanta seguidores
Cãozinho faz ensaio fofo para foto do RG Animal e encanta seguidores Estudantes brasileiros criam calculadora para aprender tabuada brincando; veja
Estudantes brasileiros criam calculadora para aprender tabuada brincando; veja Jovem que emagreceu 109 kg fica irreconhecível e motiva internautas; ‘voltei a viver’
Jovem que emagreceu 109 kg fica irreconhecível e motiva internautas; ‘voltei a viver’ SUS troca Papanicolau por novo exame menos desagradável e mais eficaz; câncer colo de útero
SUS troca Papanicolau por novo exame menos desagradável e mais eficaz; câncer colo de útero Estudantes de Medicina terão de fazer nova prova tipo “Exame da OAB”; entenda
Estudantes de Medicina terão de fazer nova prova tipo “Exame da OAB”; entenda Cai preço dos seguros dos carros mais vendidos no Brasil; Top 10
Cai preço dos seguros dos carros mais vendidos no Brasil; Top 10 Bebê sorri no ultrassom ao ouvir voz do pai e derrete corações; vídeo fofo
Bebê sorri no ultrassom ao ouvir voz do pai e derrete corações; vídeo fofo Cãozinho ferido e assustado vai à delegacia pedir socorro; tiraram chicote amarrado no pescoço
Cãozinho ferido e assustado vai à delegacia pedir socorro; tiraram chicote amarrado no pescoço Papa Francisco doou último dinheiro que tinha para caridade e jovens presos; 200 mil euros
Papa Francisco doou último dinheiro que tinha para caridade e jovens presos; 200 mil euros